
Produkter
Natriumchlorat
D'Verbindung Natriumchlorat ass en anorganescht Material mat der Standardgleichung NaClO3.Seng physesch Eegeschafte enthalen d'Wäiss a Faarf an eng kristallin Natur ze hunn déi direkt am Waasser opléist.Et gouf bekannt als hvgroskopesch (absorbéiert Feuchtigkeit aus der Loft) an der Natur.Et zerfällt iwwer 573 Kelvin fir O ze entlaaschten, a léisst NaCl hanner.
Natriumchlorat ass haaptsächlech fir Uwendungen am Bleichepulp fir Pabeier mat héijer Hellegkeet ze produzéieren.Et gëtt och benotzt fir Chlordioxid, Natriumchlorit, Perchloraten an aner Chloraten ze produzéieren.Et kann als Herbizid benotzt ginn.Mëttlerweil gëtt et an der Waasserbehandlung, Dréckerei a Fierwen, Tannage, Sprengstoff an Drocktënt benotzt.Zousätzlech kann et an der Medizin benotzt ginn, Mineralbehandlung an der Metallurgie, Abstraktioun vu Brom aus Mierwaasser, Fabrikatioun vu séchere Match a Feierwierker.


Physikalesch Eegeschafte vu Natriumchlorat
Déi physesch Eegeschafte vum Natriumchlorat sinn zimlech ähnlech wéi aner anorganesch Salzer.E puer vun hinnen sinn hei ënnendrënner opgezielt.
- Et ass eng Gerochlos Verbindung.
-seng Faarf ënnerscheet sech vu hellgiel bis wäiss kristallin fest.
- et ass ganz löslech am Waasser a méi schwéier wéi Waasser.Dofir kann et séier ënnerzegoen an opbriechen.
-Och wann et net e Sprengstoff eleng ass, kann et awer eng staark Verbrennung verursaachen wann se a Kontakt mat Waasser kommen.Et verursaacht eng héich exotherm Reaktioun.Och wann 30% vun de Molekülle am Waasser sinn, kënne se eng mächteg Oxidatiounsreaktioun verursaachen wéinst hiren inherenten Eegeschaften.
-seng Dicht ass 2,49 g / cm.
-De Kachpunkt vum Natriumchlorat ass 300 Grad C an de Schmelzpunkt ass 248 Grad C.
-et ass och löslech an e puer organeschen Léisungsmëttel wéi Glycerol a Methanol.Et ass och liicht löslech an Aceton.
-Et huet eng kubesch Kristallstruktur
Technesch Spezifizéierung
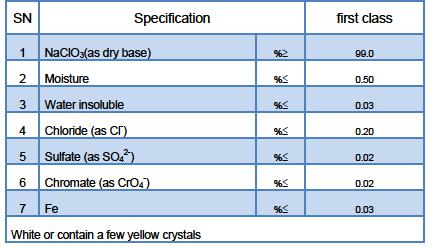
Notizen
1) all d'technesch Donnéeën uewen uginn sinn fir Är Referenz.
2) Alternativ Spezifizéierung ass wëllkomm fir weider Diskussioun.





